người ta lấy một lượng chất khí XO2 vào bình kín, tiến hành xác định khối lượng của phần khí trong bình ở điều kiện chuẩn thấy rằng: cứ 3 lít khí này tương ứng với 5,566 g. Hãy xác định công thức hóa học của chất khí đó
\(n_{XO_2}=\dfrac{3}{24,79}\left(mol\right)\)
\(\Rightarrow M_{XO_2}=\dfrac{5,566}{\dfrac{3}{24,79}}\approx46\left(g/mol\right)\)
⇒ MX + 16.2 = 46 ⇒ MX = 14
→ X là N.
Vậy: CTHH cần tìm là NO2
Đúng 2
Bình luận (0)
1.6: Hợp chất XO2 có phân tử khối gấp 2 lần phân tử khối phân tử khí Oxi. Hãy tính:
a . Phân tử khối của hợp chất XO2 ?
b .Tính nguyên tử khối cúa X và cho biết X là nguyên tố hóa học nào? Viết công thức hóa học của hợp chất XO2 ?
HUHU ="(( LẠI HELP MIK VỚI. HỨA VOTE CHO 3 BẠN ĐẦU TIÊN
a. biết \(PTK_{O_2}=2.16=32\left(đvC\right)\)
vậy \(PTK_{XO_2}=2.32=64\left(đvC\right)\)
b. ta có:
\(X+2O=64\)
\(X+2.16=64\)
\(X+32=64\)
\(X=64-32=32\left(đvC\right)\)
\(\Rightarrow X\) là lưu huỳnh \(\left(S\right)\)
CTHH của hợp chất là \(SO_2\)
Đúng 0
Bình luận (0)
chất khí A có công thức hóa học là XO2 biết rằng phân tử khí a nặng gấp 22 lần phân tử khí hidro Tìm tên nguyên tố X và công thức hóa học của khí A
a) Có 2R+(96x3)=342
Suy ra: R=27 là nhôm(Al)
b) MB=32x0,5=16
Suy ra: MA=16x2,125=34
Ta có : HuSv
5,88%=100u/34 =>u=2
94,12%=32 x 100 x v/34 => v=1
Vậy công thức hoá học của A là: H2S
Chúc bạn học tốt!
Đúng 0
Bình luận (1)
Ta có: \(M_A=22.2=44\left(g\right)\)
Mà: \(M_A=NTK_X+16.2=44\left(g\right)\)
\(\Leftrightarrow NTK_X=12\left(đvC\right)\)
Vậy X là nguyên tố cacbon (C)
Đúng 0
Bình luận (0)
Khử hoàn toàn 116(g) một oxit kim loại chưa rõ hóa trị cần dùng 44,8(lít) khí hidro ở điều kiện tiêu chuẩn xác định công thức hóa học của oxit kim loại. Biết khối lượng mol của oxit 232(g)
n oxit kim loại = 116 : 232 = 0,5 mol
n H2 = 44,8 : 22,4 = 2 mol
Gọi CTHH của oxit kl là: R\(_2O_n\)
có:
\(R_2O_n+nH_2\rightarrow2R+nH_2O\)
0,5 2
có:
2 = 0,5n
=> n = 4
Vậy CTHH của oxit kim loại là Fe3O4
Đúng 0
Bình luận (0)
Cho biết công thức hóa học hợp chất của nguyên tố X với oxi là XO2 và hợp chất của nguyên tố Y với hiđro là H2Y.
a) Xác định hóa trị của X, Y trong hợp chất?
b) Lập công thức hóa học của hợp chất tạo bởi X và Y?
a) X có hóa trị lV.
Y có hóa trị ll.
Đúng 1
Bình luận (0)
a. Ta có: \(\overset{\left(x\right)}{X}\overset{\left(II\right)}{O_2}\)
Ta lại có: x . 1 = II . 2
=> x = IV
Vậy hóa trị của X là (IV)
Ta có: \(\overset{\left(I\right)}{H_2}\overset{\left(y\right)}{Y}\)
Ta lại có: I . 2 = y . 1
=> y = II
Vậy hóa trị của Y là II
b. Gọi CTHH là: \(\overset{\left(IV\right)}{X_a}\overset{\left(II\right)}{Y_b}\)
Ta có: IV . a = II . b
=> \(\dfrac{a}{b}=\dfrac{II}{IV}=\dfrac{1}{2}\)
=> CTHH của hợp chất tạo bới X và Y là: XY2
Đúng 1
Bình luận (1)
A là khí không màu mùi hắc, rất độc và nặng hơn không khíHãy xác định công thức của hợp chất khí A, biết rằng+ A là oxit của lưu huỳnh chứa 50% oxi + 1 gam khí A chiếm thể tích 0,35 lít ở đktc A. SO B.
SO
3
C.
SO
2
D.
NO
2
Đọc tiếp
A là khí không màu mùi hắc, rất độc và nặng hơn không khí
Hãy xác định công thức của hợp chất khí A, biết rằng
+ A là oxit của lưu huỳnh chứa 50% oxi
+ 1 gam khí A chiếm thể tích 0,35 lít ở đktc
A. SO
B. SO 3
C. SO 2
D. NO 2
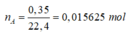
M A = m A n A = 1 0,015625 = 64 g / m o l
- Tìm số mol nguyên tử S, O trong phân tử A
Cứ 1 mol phân tử A có:
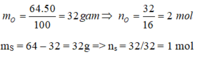
Suy ra trong 1 phân tử A có 1S và 2O, công thức của A là SO 2
Đáp án: C
Đúng 0
Bình luận (0)
Một hỗn hợp khí X gồm hai oxit là ROx và ROx+1 có tổng khối lượng là 84 gam. Ở điều kiện tiêu chuẩn, hỗn hợp X có thể tích là 28 lít. Hãy xác định công thức và phần trăm thể tích của hai oxit trong hỗn hợp X. Biết rằng R là nguyên tố thuộc nhóm VI trong bảng tuần hoàn các nguyên tố hoá học.

19,2 < R < 35,2
R là S
Xác định được: ROx là SO2 và ROx+1 là SO3
Đặt số mol của SO2 là a, số mol của SO3 là b
Ta có: a + b = 1,25 và 64a + 80b = 84
a = 1 ; b = 0,25
%V(SO2) = 80%
%V(SO3) = 20%
Đúng 0
Bình luận (0)
Một oxit kim loại có công thức là MxOy, trong đó M chiếm 72,41% khối lượng. Khử hoàn toàn oxit này bằng khí CO thu được 16,8g kim loại M. Hòa tan lượng 16,8g kim loại M bằng H2SO4 đặc nóng thu được muối M hóa trị III và 10,08 lít khí SO2(đktc) là sản phẩm khử duy nhất. a.Viết các phương trình phản ứng đã xẩy ra dưới dạng tổng quát b.Xác định công thức hóa học của oxit MxOy.
a. PTHH:
MxOy + yCO → xM + yCO2↑
2M + 6H2SO4 → M2(SO4)3 + 3SO2↑ + 6H2O
b.
2M + 6H2SO4 → M2(SO4)3 + 3SO2↑ + 6H2O
0,3 0,9 0,15 0,45 0,9
⇒MM=16,8/0,3=56 =>M là Fe.
Công thức oxit là FexOy.
Vì trong oxit kim loại Fe chiếm 72,41% khối lượng nên oxi chiếm 27,59% về khối lượng.
⇒\(\hept{\begin{cases}56x=72,41\%\left(56x+16y\right)\\16y=27,59\%\left(56x+16y\right)\end{cases}}\Rightarrow\hept{\begin{cases}x=3\\y=4\end{cases}}\)
Vậy oxit là Fe3O4.
Đúng 1
Bình luận (0)
Đốt cháy một kim loại R hóa trị 2 trong bình chứa 4,48 lít khí Oxi điều kiện tiêu chuẩn thu được 16 g oxit. Xác định R và công thức hóa học của oxit đó
Xem chi tiết
\(4R+nO_2\underrightarrow{t^0}2R_2O_n\)
\(.......0.2......\dfrac{0.4}{n}\)
\(M_{R_2O_n}=\dfrac{16}{\dfrac{0.4}{n}}=40n\)
\(\Leftrightarrow2R+16n=40n\)
\(\Leftrightarrow2R=24n\)
\(\Leftrightarrow R=12n\)
\(BL:n=2\Rightarrow R=24\)
\(CT:MgO\)
Đúng 1
Bình luận (0)
\(n_{O_2} = \dfrac{4,48}{22,4} = 0,2\ mol\)
\(2R + O_2 \xrightarrow{t^o} 2RO\)
Theo PTHH :
\(n_{Oxit} = 2n_{O_2} = 0,2.2 = 0,4\ mol\\ M_{Oxit} = R + 16 = \dfrac{16}{0,4} = 40(đvC)\\ \Rightarrow R = 24(Mg)\)
Vậy R là Mg.CTHH của oxit MgO
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Khử 4,8 gam một oxit của kim loại trong dãy điện hóa ở nhiệt độ cao cần 2,016 lít khí H2 đktc . Kim loại thu được đem hòa tan trong dung dịch HCl thu được 1,344 lít khí H2 đktc . Hãy xác định công thức hóa học của oxit đã dùng: A. Fe2O3 B. MgO C. Fe3O4 D. Al2O3
Đọc tiếp
Khử 4,8 gam một oxit của kim loại trong dãy điện hóa ở nhiệt độ cao cần 2,016 lít khí H2 đktc . Kim loại thu được đem hòa tan trong dung dịch HCl thu được 1,344 lít khí H2 đktc . Hãy xác định công thức hóa học của oxit đã dùng:
A. Fe2O3
B. MgO
C. Fe3O4
D. Al2O3
Đáp án A
Oxit chưa biết của kim loại nào → Gọi MxOy
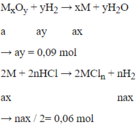
Mà : 56ax + 16ay = 4,8
→ ax = 0,06
→ x : y = ax : ay = 0,06 : 0,09 = 2 : 3 => M2O3
→ n = 0,12 : 0,06 = 2 => M hóa trị II
→ Chỉ có Fe thỏa mãn vì nó có hai hóa trị
Lưu ý: Bài toán này dễ nhầm lẫn nếu không để ý sự thay đổi hóa trị ở 2 phương trình.
Đúng 0
Bình luận (0)


























